Arze-Ject-A
نام عمومی: تریامسینولون استونید
فرم دوز: تعلیق تزریقی
در این صفحه
- توضیحات
- فارماکولوژی بالینی
- موارد مصرف و استفاده از آن
- موارد منع مصرف
- هشدارها
- موارد احتیاطی
- اطلاعات مشاوره بیمار
- تداخلات دارویی
- واکنشهای جانبی / عوارض جانبی
- مصرف بیش از حد دارو
- مقدار و نحوه مصرف
- نحوه تهیه / ذخیره سازی و نحوه مدیریت
——————– تزریق Kenalog®-40 (سوسپانسیون تزریقی تریامسینولون استونید ، USP) ————– ——
برای استفاده در نوزادان نیست
حاوی بنزیل الکل است
فقط برای استفاده عضلانی یا داخل مفصلی
نه برای استفاده در داخل ، داخلی ، داخل چشم ، اپیدورال ، یا استفاده در داخل
توضیحات Arze-Ject-A
Kenalog ® -40 تزریق (سوسپانسیون تزریقی تریامسینولون استونید ، USP) یک کورتیکواستروئید گلوکوکورتیکوئید مصنوعی با عملکرد ضد التهابی است. این فرم فقط برای استفاده در عضلات و داخل مفصل قابل استفاده است. این فرمول برای تزریق داخلی نیست.
هر میلی لیتر از سوسپانسیون آب استریل 40 میلی گرم تریامسینولون استونید ، با 0.65٪ کلرید سدیم برای ایزوتونیک بودن ، 0.99٪ (وزنی / وزنی) الکل بنزیل به عنوان نگهدارنده ، 0.75٪ کربوکسی متیل سلولز سدیم و 0.04٪ پلی سوربات 80 فراهم می کند. هیدروکسید سدیم یا اسید کلریدریک ممکن است برای تنظیم pH به 5.0 تا 7.5 وجود داشته باشد. در زمان تولید ، هوای ظرف با نیتروژن جایگزین می شود.
نام شیمیایی تریامسینولون استونید 9-Fluoro-11β ، 16α ، 17،21-tetrahydroxypregna-1،4-diene-3،20-dione cyclic 16،17-acetal با استون است. فرمول ساختاری آن عبارت است از:
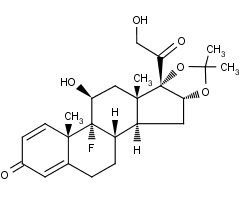
تریامسینولون استونید به صورت پودری متبلور به رنگ سفید تا کرم و بوی کمی بیش از حد ایجاد می شود و عملا در آب حل نمی شود و در الکل بسیار محلول است.
Arze-Ject-A – داروسازی بالینی
گلوكوكورتيكوئيدها ، به طور طبيعي و مصنوعي ، استروئيدهاي فوق كليوي هستند كه به راحتي از دستگاه گوارش جذب مي شوند.
گلوکوکورتیکوئیدهای طبیعی (هیدروکورتیزون و کورتیزون) که دارای خواص نگهدارنده نمک نیز هستند ، به عنوان درمان جایگزینی در موارد کمبود آدرنال استفاده می شود. از آنالوگ های مصنوعی مانند تریامسینولون در درجه اول برای اثرات ضد التهابی در اختلالات بسیاری از سیستم های اندام استفاده می شود.
تزریق Kenalog-40 دارای اثر طولانی تری است که ممکن است در طی چند هفته ادامه یابد. مطالعات نشان می دهد که به دنبال یک دوز عضلانی از 60 میلی گرم تا 100 میلی گرم تریامسینولون استونید ، سرکوب غده فوق کلیه در طی 24 تا 48 ساعت اتفاق می افتد و سپس به تدریج به حالت نرمال برمی گردد ، معمولاً طی 30 تا 40 روز. این یافته ارتباط تنگاتنگی با طولانی شدن مدت زمان انجام اقدامات درمانی با دارو دارد.
موارد مصرف و استفاده برای Arze-Ject-A
عضلانی
در مواردی که درمان خوراکی امکان پذیر نیست ، درمان کورتیکواستروئید تزریقی ، از جمله Kenalog-40 Injection (سوسپانسیون تزریقی تریامسینولون استونید ، USP) برای استفاده در عضلات نشان داده شده است به شرح زیر است:
حالات آلرژیک: کنترل شرایط آلرژیک شدید یا ناتوان کننده و غیرقابل حل در آزمایش های کافی درمان متداول در آسم ، درماتیت آتوپیک ، درماتیت تماسی ، واکنش های حساسیت دارویی ، رینیت آلرژیک چند ساله یا فصلی ، بیماری سرمی ، واکنش های انتقال خون.
بیماریهای پوستی: درماتیت بولوز هرپتیفورمیس ، اریترودرمای لایه بردار ، مایکوز فونگوئیدس ، پمفیگوس ، اریتم مولتی فرم شدید (سندرم استیونس-جانسون).
اختلالات غدد درون ریز: نارسایی غده فوق کلیوی یا ثانویه (هیدروکورتیزون یا کورتیزون داروی انتخابی است ؛ از آنالوگهای مصنوعی ممکن است در صورت استفاده همراه با مینرالوکورتیکوئیدها استفاده شود ؛ در نوزادی ، مکمل مینرالوکورتیکوئید از اهمیت ویژه ای برخوردار است) ، هایپرپلازی مادرزادی آدرنال ، هیپرکلسمی مرتبط با سرطان ، تیروئیدیت غیرقوایی.
بیماری های دستگاه گوارش: برای تسریع بیمار در یک دوره حساس بیماری در ورم روده منطقه و کولیت اولسراتیو.
اختلالات هماتولوژیک: کم خونی همولیتیک اکتسابی (خود ایمنی) ، کم خونی Diamond-Blackfan ، آپلازی سلولهای قرمز خالص ، موارد منتخب ترومبوسیتوپنی ثانویه.
متفرقه: تریکینوز همراه با درگیری عصبی یا میوکارد ، مننژیت سل با بلوک زیر عنکبوتیه یا بلوک قریب الوقوع در صورت استفاده با شیمی درمانی مناسب ضد سل.
بیماریهای نئوپلاستیک: برای مدیریت تسکینی سرطان خون و لنفوم.
سیستم عصبی: تشدید حاد بیماری مولتیپل اسکلروزیس. ادم مغزی همراه با تومور مغزی یا کرانیوتومی اولیه یا متاستاتیک.
بیماری های چشمی: چشم های دلسوز ، آرتریت تمپورال ، یووئیت و التهابات چشمی که به کورتیکواستروئیدهای موضعی پاسخ نمی دهند.
بیماری های کلیوی: برای القا di ادرار یا بهبودی پروتئینوریا در سندرم نفروتیک ایدیوپاتیک یا به دلیل لوپوس اریتماتوز.
بیماری های تنفسی: بریلیوز ، سل ریوی کامل یا پخش شده در صورت استفاده همزمان با شیمی درمانی مناسب ضد سل ، پنومونی ائوزینوفیل ایدیوپاتیک ، سارکوئیدوز علامتی.
اختلالات روماتیسمی: به عنوان درمان کمکی برای تجویز کوتاه مدت (برای جابجایی بیمار در یک دوره حاد یا تشدید) در آرتریت حاد نقرس. کاردیت حاد روماتیسمی ؛ اسپوندیلیت آنکیلوزان؛ آرتریت پسوریازیس ؛ آرتریت روماتوئید ، از جمله آرتریت روماتوئید نوجوانان (موارد انتخاب شده ممکن است به درمان نگهدارنده با دوز پایین نیاز داشته باشند). برای درمان درماتومیوزیت ، پلی میوزیت و لوپوس اریتماتوز سیستمیک.
داخل مفصلی
تجویز داخل مفصلی یا بافت نرم تزریق Kenalog-40 به عنوان درمان کمکی برای تجویز کوتاه مدت نشان داده می شود (برای تند کردن بیمار نسبت به اپیزود حاد یا تشدید) در آرتریت حاد نقرس ، بورسیت حاد و تحت حاد ، تنوسینوویت غیر اختصاصی حاد ، اپی کندیلیت ، آرتریت روماتوئید ، سینوویت یا آرتروز.
موارد منع مصرف
تزریق Kenalog-40 در بیمارانی که نسبت به سایر اجزای این محصول حساسیت زیادی دارند منع مصرف دارد (به هشدارها: عمومی ).
آماده سازی کورتیکواستروئیدهای عضلانی برای پورپورای ایدیوپاتیک ترومبوسیتوپنیک منع شده است.
هشدارها
واکنشهای جانبی جدی نورولوژیک با تجویز اپیدورال
رویدادهای جدی عصبی ، که برخی منجر به مرگ شده اند ، با تزریق کورتیکواستروئیدها به روش اپیدورال گزارش شده است ( هشدارها: Neurologic ). وقایع خاص گزارش شده شامل سکته مغزی نخاع ، پاراپلژی ، کوادریپلژی ، کوری قشر مغز و سکته مغزی است. این موارد جدی نورولوژیک با استفاده از فلوروسکوپی و بدون آن گزارش شده است. ایمنی و اثربخشی تجویز کورتیکواستروئیدها در اپیدورال مشخص نشده است و کورتیکواستروئیدها برای این استفاده تأیید نشده اند.
عمومی
قرار گرفتن در معرض مقادیر بیش از حد الکل بنزیل با مسمومیت (افت فشار خون ، اسیدوز متابولیک) ، به ویژه در نوزادان و افزایش بروز کرنیکتروس ، به ویژه در نوزادان نارس کوچک همراه است. گزارش های نادری از مرگ ، در درجه اول در نوزادان نارس ، در ارتباط با قرار گرفتن در معرض مقادیر بیش از حد بنزیل الکل گزارش شده است. مقدار بنزیل الکل از داروها در مقایسه با مقدار دریافت شده در محلول های شستشوی حاوی بنزیل الکل معمولاً ناچیز تلقی می شود. تجویز دوزهای بالای داروهای حاوی این ماده نگهدارنده باید مقدار کل الکل بنزیل تجویز شده را در نظر بگیرد. مقدار الکل بنزیل که ممکن است در آن سمیت ایجاد شود مشخص نیست. اگر بیمار بیش از دوزهای توصیه شده یا سایر داروهای حاوی این ماده نگهدارنده نیاز دارد ، پزشک باید بار متابولیکی روزانه بنزیل الکل را از این منابع ترکیبی در نظر بگیرد ( اقدامات احتیاطی: استفاده از کودکان ).
موارد نادر آنافیلاکسی در بیمارانی که تحت درمان با کورتیکواستروئید قرار گرفته اند رخ داده است ( ADVERSE واکنشها ). مواردی از آنافیلاکسی جدی ، از جمله مرگ ، در افرادی که تزریق تریامسینولون استونید دریافت کرده اند ، بدون در نظر گرفتن مسیر تجویز ، گزارش شده است.
از آنجا که Kenalog-40 Injection (سوسپانسیون تزریقی تریامسینولون استونید ، USP) یک سوسپانسیون است ، بنابراین نیست باید به صورت داخل وریدی تجویز شود.
مگر اینکه تزریق عضلانی عمیق انجام شود ، احتمالاً آتروفی موضعی رخ می دهد. (برای توصیه های مربوط به تکنیک های تزریق ، DOSAGE AND مدیریت .)) به دلیل بروز آتروفی موضعی به طور قابل توجهی در هنگام مواد به ناحیه دلتوئید تزریق می شود ، باید از این محل تزریق به نفع ناحیه گلوتئال جلوگیری شود.
افزایش دوز کورتیکواستروئیدهایی که به سرعت در حال انجام هستند ، در بیمارانی که تحت درمان با کورتیکواستروئید قرار دارند ، تحت هرگونه استرس غیرعادی قبل ، حین و بعد از وضعیت استرس زا نشان داده می شود. تزریق Kenalog-40 یک آماده سازی طولانی مدت است و برای استفاده در شرایط استرس حاد مناسب نیست. برای جلوگیری از نارسایی آدرنال ناشی از دارو ، ممکن است در زمان استرس (مانند ضربه ، جراحی یا بیماری شدید) هم در حین درمان با تزریق Kenalog-40 و هم به مدت یک سال دوز حمایتی مورد نیاز باشد.
نتایج حاصل از یک مطالعه چند مرکزی ، تصادفی و کنترل شده با دارونما با متیل پردنیزولون همی سوسینات ، یک کورتیکواستروئید داخل وریدی ، افزایش مرگ و میر در اوایل (در 2 هفته) و در اواخر (در 6 ماه) را در بیماران مبتلا به ترومای جمجمه نشان داد که علائم واضح دیگری برای درمان کورتیکواستروئید داشته باشید. از دوزهای بالای کورتیکواستروئیدهای سیستمیک ، از جمله تزریق Kenalog-40 ، برای درمان آسیب مغزی ضربه ای استفاده نمی شود.
قلبی-کلیوی
دوزهای متوسط و زیاد کورتیکواستروئیدها می توانند باعث افزایش فشار خون ، احتباس نمک و آب و افزایش دفع پتاسیم شوند. این تأثیرات کمتر در مشتقات مصنوعی اتفاق می افتد مگر در مواردی که در مقادیر زیاد استفاده شود. محدودیت نمک و مکمل پتاسیم در رژیم غذایی ممکن است لازم باشد ( احتیاطات را ببینید). همه کورتیکواستروئیدها باعث افزایش دفع کلسیم می شوند.
گزارش های ادبیات حاکی از وجود ارتباط آشکاری بین استفاده از کورتیکواستروئیدها و پارگی دیواره آزاد بطن چپ پس از سکته قلبی اخیر است. بنابراین ، در این بیماران باید با احتیاط زیادی از درمان با کورتیکواستروئیدها استفاده شود.
غدد درون ریز
کورتیکواستروئیدها می توانند سرکوب محور هیپوتالاموس-هیپوفیز-آدرنال برگشت پذیر (HPA) را ایجاد کنند که احتمال بروز نارسایی گلوکوکورتیکواستروئید پس از قطع درمان وجود دارد.
ترخیص متابولیک کورتیکواستروئیدها در بیماران کم کاری تیروئید کاهش یافته و در بیماران هیپرتیروئید افزایش می یابد. تغییر در وضعیت تیروئید بیمار ممکن است نیاز به تنظیم دوز داشته باشد.
عفونت
عمومی
بیمارانی که از کورتیکواستروئید استفاده می کنند نسبت به افراد سالم مستعد ابتلا به عفونت هستند. در صورت استفاده از کورتیکواستروئیدها ممکن است مقاومت و عدم توانایی در محلی سازی عفونت وجود داشته باشد. عفونت با هر پاتوژن (ویروسی ، باکتریایی ، قارچی ، تک یاخته ای یا هلمینتیک) در هر مکان از بدن ممکن است با استفاده از کورتیکواستروئیدها به تنهایی یا در ترکیب با سایر عوامل سرکوب کننده سیستم ایمنی همراه باشد. این عفونت ها ممکن است خفیف تا شدید باشند. با افزایش دوزهای کورتیکواستروئیدها ، میزان بروز عوارض عفونی افزایش می یابد. کورتیکواستروئیدها همچنین ممکن است برخی از علائم عفونت فعلی را پنهان کنند.
عفونت های قارچی
کورتیکواستروئیدها ممکن است عفونتهای قارچی سیستمیک را تشدید کنند و بنابراین نباید در حضور چنین عفونتهایی استفاده شود ، مگر اینکه به آنها برای کنترل واکنشهای دارویی نیاز باشد. مواردی گزارش شده است که مصرف همزمان آمفوتریسین B و هیدروکورتیزون با بزرگ شدن قلب و نارسایی احتقانی قلب همراه بوده است ( را ببینید) احتیاط ها: تداخلات دارویی : تزریق آمفوتریسین B و عوامل تخریب کننده پتاسیم ).
عوامل بیماری زای ویژه
بیماری نهفته ممکن است فعال شود یا ممکن است به دلیل عوامل بیماری زا ، از جمله موارد ناشی از آمیب ، کاندیدا ، کریپتوکوک ، مایکوباکتریوم ، نوکاردیا ، پنوموسیستیس ، تشدید عفونت های همزمان باشد. یا توکسوپلاسما.
توصیه می شود قبل از شروع درمان با کورتیکواستروئید در هر بیمار که مدتی را در مناطق گرمسیری یا هر بیمار مبتلا به اسهال غیرقابل توضیح گذرانده است ، آمبیازیس نهفته یا آمبیازیس فعال منتفی شود.
به همین ترتیب ، کورتیکواستروئیدها باید در بیماران مبتلا به آلودگی شناخته شده یا مشکوک استرانگلیوئید (کرم نخ) با احتیاط کامل استفاده شود. در چنین بیمارانی ، سرکوب سیستم ایمنی ناشی از کورتیکواستروئید ممکن است به استرانگیلوئیدها منجر به ضد عفونی و انتشار با مهاجرت گسترده لارو شود که اغلب با انتروکولیت شدید و سپتی سمی گرم منفی بالقوه همراه است.
از کورتیکواستروئیدها نباید در مالاریای مغزی استفاده شود.
سل
استفاده از داروهای کورتیکواستروئید در بیماران مبتلا به سل فعال باید محدود به موارد سل کامل یا پراکنده باشد که در آن کورتیکواستروئید برای مدیریت بیماری همراه با یک رژیم ضد سل مناسب استفاده شود. اگر کورتیکواستروئیدها در بیماران مبتلا به سل نهفته یا واکنش توبرکولین نشان داده شوند ، مشاهده دقیق از آنجا که ممکن است دوباره فعال سازی بیماری رخ دهد ، لازم است. در طول درمان طولانی مدت با کورتیکواستروئید ، این بیماران باید کموپروفیلاکسی دریافت کنند.
واکسیناسیون
تجویز واکسن های زنده و زنده ضعیف شده در بیمارانی که دوزهای سرکوب کننده سیستم ایمنی کورتیکواستروئیدها دریافت می کنند منع مصرف دارد. واکسن های کشته شده یا غیرفعال شده ممکن است تجویز شوند. با این حال ، پاسخ به این واکسن ها را نمی توان پیش بینی کرد. ممکن است در بیمارانی که کورتیکواستروئیدها را به عنوان درمان جایگزینی ، مثلاً برای بیماری آدیسون دریافت می کنند ، روش ایمن سازی انجام شود.
عفونت های ویروسی
آبله مرغان و سرخک می توانند روند جدی تر یا حتی کشنده ای را در بیماران کودکان و بزرگسالان با کورتیکواستروئیدها داشته باشند. در بیماران اطفال و بزرگسالان که این بیماری ها را نداشته اند ، باید مراقبت های ویژه ای انجام شود تا از مواجهه با آنها جلوگیری شود. سهم بیماری زمینه ای و / یا درمان قبلی کورتیکواستروئید در خطر نیز مشخص نیست. اگر در معرض آبله مرغان قرار گیرد ، ممکن است پروفیلاکسی با گلوبولین ایمنی واریسلا زوستر (VZIG) نشان داده شود. اگر در معرض سرخک قرار گیرد ، ممکن است پروفیلاکسی با ایمونوگلوبولین (IG) نشان داده شود. (برای اطلاعات کامل در مورد تجویز VZIG و IG به درج بسته مربوطه مراجعه کنید.) در صورت ایجاد آبله مرغان ، درمان با داروهای ضد ویروسی باید در نظر گرفته شود.
Neurologic
تزریق اپیدورال و داخل روده ای این محصول توصیه نمی شود. گزارشات مربوط به وقایع پزشکی جدی ، از جمله مرگ ، با مسیرهای اپیدورال و داخل مجرای تجویز کورتیکواستروئید همراه بوده است ( ADVERSE مراجعه کنید) REACTIONS : دستگاه گوارش و Neurologic / Psychiatric ).
چشم
استفاده از کورتیکواستروئیدها ممکن است باعث ایجاد آب مروارید زیر کپسول خلفی ، گلوکوم با آسیب احتمالی به اعصاب بینایی شود و ایجاد عفونت های ثانویه چشمی ناشی از باکتری ها ، قارچ ها یا ویروس ها را افزایش دهد. استفاده از کورتیکواستروئیدهای خوراکی در درمان نوریت بینایی توصیه نمی شود و ممکن است منجر به افزایش احتمال بروز قسمت های جدید شود. از کورتیکواستروئیدها نباید در هرپس سیمپلکس فعال چشم استفاده شود.
مطالعات کافی برای اثبات ایمنی تزریق Kenalog Injection توسط تزریقات داخل حفره ای ، زیر ملتحمه ، زیر تنون ، رتروبولبار و داخل چشم (داخل رحمی) انجام نشده است. اندوفتالمیت ، التهاب چشم ، افزایش فشار داخل چشم و اختلالات بینایی از جمله از دست دادن بینایی با تجویز داخل رحمی گزارش شده است. تجویز Kenalog Injection از طریق چشم یا در توربین های بینی توصیه نمی شود.
تزریق داخل چشم فرمولاسیون کورتیکواستروئید حاوی بنزیل الکل ، مانند Kenalog Injection ، به دلیل سمیت بالقوه ناشی از الکل بنزیل توصیه نمی شود.
موارد احتیاطی
عمومی
این محصول ، مانند بسیاری دیگر از ترکیبات استروئیدی ، به گرما حساس است. بنابراین ، در صورت استریل کردن قسمت بیرونی ویال ، نباید اتوکلاو شود.
برای کنترل وضعیت تحت درمان باید از کمترین دوز ممکن کورتیکواستروئید استفاده شود. هنگامی که کاهش دوز ممکن است ، کاهش باید به تدریج انجام شود.
از آنجا که عوارض درمان با گلوکوکورتیکوئیدها به اندازه دوز و مدت زمان درمان بستگی دارد ، در مورد دوز و مدت درمان و در مورد اینکه آیا درمان روزانه یا متناوب است باید در هر مورد تصمیم خطر / فایده گرفته شود. باید استفاده شود.
گزارش شده است که سارکوم Kaposi در بیمارانی که تحت درمان با کورتیکواستروئید قرار دارند ، اغلب در موارد مزمن رخ می دهد. قطع مصرف کورتیکواستروئیدها ممکن است منجر به بهبود بالینی شود.
قلبی-کلیوی
از آنجا که احتباس سدیم همراه با ادم و از دست دادن پتاسیم در بیماران دریافت کننده کورتیکواستروئیدها ممکن است رخ دهد ، از این عوامل باید در بیماران مبتلا به نارسایی احتقانی قلب ، فشار خون بالا یا نارسایی کلیوی با احتیاط استفاده شود.
غدد درون ریز
ممکن است با کاهش تدریجی دوز ، نارسایی ثانویه آدرنال مغزی ناشی از دارو به حداقل برسد. این نوع نارسایی نسبی ممکن است ماهها پس از قطع درمان ادامه یابد. بنابراین ، در هر شرایط استرسی که در آن دوره اتفاق می افتد ، هورمون درمانی باید دوباره جایگزین شود. از آنجا که ممکن است ترشح مینرالوکورتیکوئید مختل شود ، باید همزمان نمک و / یا مینرال کورتیکویید تجویز شود.
دستگاه گوارش
استروئیدها باید با احتیاط در زخم معده فعال یا نهفته ، دیورتیکولیت ، آناستوموز روده تازه و کولیت اولسراتیو غیر اختصاصی استفاده شوند ، زیرا ممکن است خطر سوراخ شدن را افزایش دهند.
علائم تحریک صفاقی به دنبال سوراخ شدن دستگاه گوارش در بیمارانی که کورتیکواستروئید دریافت می کنند ممکن است کم باشد یا وجود نداشته باشد.
در بیماران مبتلا به سیروز اثر کورتیکواستروئیدها افزایش یافته است.
تجویز داخل مفصلی و بافت نرم
کورتیکواستروئیدهای تزریق داخل مفصلی ممکن است به طور سیستماتیک جذب شوند.
معاینه مناسب هر مایع مفصلی موجود برای حذف فرآیند سپتیک ضروری است.
افزایش قابل توجه درد همراه با تورم موضعی ، محدودیت بیشتر حرکت مفصل ، تب و کسالت بیانگر آرتروز سپتیک است. در صورت بروز این عارضه و تأیید تشخیص سپسیس ، باید درمان ضد میکروبی مناسب آغاز شود.
از تزریق استروئید به محل آلوده خودداری شود. تزریق موضعی استروئید در مفصلی که قبلاً آلوده شده است معمولاً توصیه نمی شود.
تزریق کورتیکواستروئید به مفاصل ناپایدار به طور کلی توصیه نمی شود.
تزریق داخل مفصلی ممکن است منجر به آسیب به بافت های مفصلی شود ( پیشنهاد ” واکنشها : اسکلتی عضلانی ).
اسکلت عضلانی
کورتیکواستروئیدها هم از طریق تأثیر بر تنظیم کلسیم (یعنی کاهش جذب و افزایش دفع) و هم از طریق مهار عملکرد استئوبلاست باعث کاهش تشکیل استخوان و افزایش تحلیل استخوان می شوند. این ، همراه با کاهش ماتریس پروتئین استخوان ثانویه به افزایش کاتابولیسم پروتئین و کاهش تولید هورمون جنسی ، ممکن است منجر به مهار رشد استخوان در بیماران کودکان و بروز پوکی استخوان در هر سنی شود. قبل از شروع درمان با کورتیکواستروئید ، باید به بیماران در معرض خطر پوکی استخوان (یعنی زنان یائسه) توجه ویژه شود.
روانپزشکی عصبی
اگرچه آزمایشات بالینی کنترل شده نشان داده است که کورتیکواستروئیدها در سرعت بخشیدن به تشدید حاد بیماری مولتیپل اسکلروزیس موثر هستند ، اما نشان نمی دهد که آنها بر نتیجه نهایی یا سابقه طبیعی بیماری تأثیر می گذارند. مطالعات نشان می دهد که دوزهای نسبتاً زیاد کورتیکواستروئیدها برای نشان دادن تأثیر قابل توجهی ضروری است. ( DOSAGE و مدیریت .)
میوپاتی حاد با استفاده از دوزهای بالای کورتیکواستروئید مشاهده شده است ، که اغلب در بیماران مبتلا به اختلالات انتقال عصبی عضلانی (به عنوان مثال ، میاستنی گراویس) یا در بیمارانی که تحت درمان همزمان با داروهای انسداد عصبی عضلانی (به عنوان مثال ، پانکورونیوم) مشاهده می شوند ، مشاهده می شود. . این میوپاتی حاد عمومی است ، ممکن است عضلات چشمی و تنفسی را درگیر کند و منجر به کوادریپارزی شود. ممکن است افزایش کراتینین کیناز رخ دهد. بهبود یا بهبودی بالینی پس از قطع کورتیکواستروئیدها ممکن است هفته ها تا سالها نیاز داشته باشد.
اختلالات روانپزشکی ممکن است هنگام استفاده از کورتیکواستروئیدها ظاهر شود ، از سرخوشی ، بی خوابی ، تغییرات خلقی ، تغییرات شخصیتی و افسردگی شدید گرفته تا تظاهرات روان پریشی صریح. همچنین ، بی ثباتی عاطفی یا گرایش های روانی ممکن است توسط کورتیکواستروئیدها تشدید شود.
چشم
فشار داخل چشم ممکن است در بعضی از افراد افزایش یابد. اگر درمان با استروئید بیش از 6 هفته ادامه یابد ، باید فشار داخل چشم کنترل شود.
اطلاعات برای بیماران
باید به بیماران هشدار داده شود که استفاده از کورتون را به طور ناگهانی یا بدون نظارت پزشکی قطع نکنند ، به هر یک از مراقبان پزشکی توصیه کنند که از داروهای کورتون استفاده می کنند و در صورت بروز تب یا علائم دیگر ، بلافاصله به دنبال مشاوره پزشکی باشند. عفونت.
به افرادی که کورتیکواستروئید مصرف می کنند باید هشدار داده شود تا از قرار گرفتن در معرض آبله مرغان یا سرخک خودداری کنند. همچنین باید به بیماران توصیه شود که در صورت مواجهه ، بدون تأخیر باید از مشاوره پزشکی استفاده کرد.
تداخلات دارویی
آمینوگلوتتیمید: آمینوگلوتتیمید ممکن است منجر به از بین رفتن سرکوب غده فوق کلیه ناشی از کورتیکواستروئید شود.
تزریق آمفوتریسین B و عوامل تخریب کننده پتاسیم: هنگامی که کورتیکواستروئیدها به طور همزمان با عوامل تخلیه کننده پتاسیم (به عنوان مثال آمفوتریسین B ، ادرار آورها) تجویز می شوند ، بیماران باید برای پیشرفت از نزدیک مشاهده شوند هیپوکالمی مواردی گزارش شده است که مصرف همزمان آمفوتریسین B و هیدروکورتیزون با بزرگ شدن قلب و نارسایی احتقانی قلب همراه بوده است.
آنتی بیوتیک ها: گزارش شده است که آنتی بیوتیک های ماکرولید باعث کاهش چشمگیر ترشح کورتیکواستروئید می شوند.
آنتی کولین استرازها: استفاده همزمان از داروهای آنتی کولین استراز و کورتیکواستروئیدها ممکن است ضعف شدیدی را در بیماران مبتلا به میاستنی گراویس ایجاد کند. در صورت امکان ، حداقل 24 ساعت قبل از شروع درمان با کورتیکواستروئید ، عوامل آنتی کولین استراز باید ترک شوند.
ضدانعقاد ، خوراکی: مدیریت همزمان کورتیکواستروئیدها و وارفارین معمولاً منجر به مهار پاسخ به وارفارین می شود ، اگرچه گزارش های متناقضی نیز وجود داشته است. بنابراین ، باید شاخص های انعقادی را مرتباً کنترل کرد تا اثر ضد انعقادی مطلوب حفظ شود.
ضد دیابت: از آنجا که کورتیکواستروئیدها ممکن است غلظت گلوکز خون را افزایش دهند ، ممکن است تنظیمات دوز عوامل ضد دیابت لازم باشد.
داروهای ضد سل: غلظت سرمی ایزونیازید ممکن است کاهش یابد.
کلستیرامین: کلستیرامین ممکن است پاکسازی کورتیکواستروئیدها را افزایش دهد.
سیکلوسپورین: افزایش فعالیت هر دو سیکلوسپورین و کورتیکواستروئیدها ممکن است هنگام استفاده همزمان از این دو رخ دهد. با این استفاده همزمان تشنج گزارش شده است.
گلیكوزیدهای دیجیتال: بیماران مبتلا به گلیكوزید دیجیتال ممكن است به دلیل هیپوكالمی در معرض خطر آریتمی قرار داشته باشند.
استروژن ها ، از جمله داروهای ضد بارداری خوراکی: استروژن ها ممکن است متابولیسم کبدی برخی از کورتیکواستروئیدها را کاهش دهند ، در نتیجه اثر آنها را افزایش می دهند.
القا کننده های آنزیم کبدی (به عنوان مثال ، باربیتورات ها ، فنی توئین ، کاربامازپین ، ریفامپین): داروهایی که باعث فعالیت آنزیم متابولیزه کننده داروی میکروزومال کبدی می شوند ، می توانند متابولیسم کورتیکواستروئیدها را افزایش دهند و نیاز به دوز دارو دارند کورتیکواستروئید افزایش یابد.
کتوکونازول: کتوکونازول گزارش شده است که متابولیسم برخی کورتیکواستروئیدها را تا 60٪ کاهش می دهد ، که منجر به افزایش خطر عوارض جانبی کورتیکواستروئید می شود.
داروهای ضد التهاب غیر استروئیدی (NSAID): مصرف همزمان آسپیرین (یا داروهای ضد التهاب غیراستروئیدی) و کورتیکواستروئیدها خطر عوارض گوارشی را افزایش می دهد. آسپرین باید با احتیاط همراه با کورتیکواستروئیدها در هیپوپروترومبینمی مصرف شود. پاکسازی سالیسیلات ها ممکن است با استفاده همزمان از کورتیکواستروئیدها افزایش یابد.
آزمایشات پوستی: کورتیکواستروئیدها ممکن است واکنش های آزمایشات پوستی را سرکوب کنند.
واکسن ها: بیمارانی که تحت درمان طولانی مدت با کورتیکواستروئید هستند ممکن است به دلیل مهار پاسخ آنتی بادی ، پاسخ کمتری به توکسوئیدها و واکسن های زنده یا غیرفعال نشان دهند. کورتیکواستروئیدها همچنین ممکن است تکثیر برخی موجودات موجود در واکسن های ضعیف شده زنده را تقویت کنند. تجویز معمول واکسن ها یا سموم باید تا زمانی که درمان کورتیکواستروئید قطع نشود به تعویق بیفتد ( هشدارها را ببینید : عفونت ها : واکسیناسیون ).
سرطان زایی ، جهش زایی ، اختلال در باروری
هیچ مطالعه کافی برای تعیین اینکه آیا کورتیکواستروئیدها پتانسیل سرطان زایی یا جهش زایی دارند ، روی حیوانات انجام نشده است.
استروئیدها ممکن است باعث تحرک و تعداد اسپرماتوزوئیدها در بعضی از بیماران شوند.
بارداری
Teratogenic Effects: Pregnancy Category C
Corticosteroids have been shown to be teratogenic in many species when given in doses equivalent to the human dose. Animal studies in which corticosteroids have been given to pregnant mice, rats, and rabbits have yielded an increased incidence of cleft palate in the offspring. هیچ مطالعه کافی و کنترل شده ای روی زنان باردار وجود ندارد. Corticosteroids should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus. Infants born to mothers who have received corticosteroids during pregnancy should be carefully observed for signs of hypoadrenalism.
مادران پرستار
Systemically administered corticosteroids appear in human milk and could suppress growth, interfere with endogenous corticosteroid production, or cause other untoward effects. Caution should be exercised when corticosteroids are administered to a nursing woman.
استفاده از کودکان
This product contains benzyl alcohol as a preservative. Benzyl alcohol, a component of this product, has been associated with serious adverse events and death, particularly in pediatric patients. The “gasping syndrome” (characterized by central nervous system depression, metabolic acidosis, gasping respirations, and high levels of benzyl alcohol and its metabolites found in the blood and urine) has been associated with benzyl alcohol99 mg/kg/day in neonates and low-birth-weight neonates. Additional symptoms may include gradual neurological deterioration, seizures, intracranial hemorrhage, hematologic abnormalities, skin breakdown, hepatic and renal failure, hypotension, bradycardia, and cardiovascular collapse. Although normal therapeutic doses of this product deliver amounts of benzyl alcohol that are substantially lower than those reported in association with the “gasping syndrome,” the minimum amount of benzyl alcohol at which toxicity may occur is not known. Premature and low-birth-weight infants, as well as patients receiving high dosages, may be more likely to develop toxicity. Practitioners administering this and other medications containing benzyl alcohol should consider the combined daily metabolic load of benzyl alcohol from all sources.
The efficacy and safety of corticosteroids in the pediatric population are based on the well-established course of effect of corticosteroids which is similar in pediatric and adult populations. Published studies provide evidence of efficacy and safety in pediatric patients for the treatment of nephrotic syndrome (>2 years of age), and aggressive lymphomas and leukemias (>1 month of age). Other indications for pediatric use of corticosteroids, eg, severe asthma and wheezing, are based on adequate and well-controlled trials conducted in adults, on the premises that the course of the diseases and their pathophysiology are considered to be substantially similar in both populations.
The adverse effects of corticosteroids in pediatric patients are similar to those in adults (see ADVERSE REACTIONS). Like adults, pediatric patients should be carefully observed with frequent measurements of blood pressure, weight, height, intraocular pressure, and clinical evaluation for the presence of infection, psychosocial disturbances, thromboembolism, peptic ulcers, cataracts, and osteoporosis. Pediatric patients who are treated with corticosteroids by any route, including systemically administered corticosteroids, may experience a decrease in their growth velocity. This negative impact of corticosteroids on growth has been observed at low systemic doses and in the absence of laboratory evidence of HPA axis suppression (ie, cosyntropin stimulation and basal cortisol plasma levels). Growth velocity may therefore be a more sensitive indicator of systemic corticosteroid exposure in pediatric patients than some commonly used tests of HPA axis function. The linear growth of pediatric patients treated with corticosteroids should be monitored, and the potential growth effects of prolonged treatment should be weighed against clinical benefits obtained and the availability of treatment alternatives. In order to minimize the potential growth effects of corticosteroids, pediatric patients should be titrated to the lowest effective dose.
استفاده از سالخوردگی
No overall differences in safety or effectiveness were observed between elderly subjects and younger subjects, and other reported clinical experience has not identified differences in responses between the elderly and younger patients, but greater sensitivity of some older individuals cannot be ruled out.
واکنشهای جانبی
(listed alphabetically under each subsection)
The following adverse reactions may be associated with corticosteroid therapy:
Allergic reactions: Anaphylaxis including death, angioedema.
Cardiovascular: Bradycardia, cardiac arrest, cardiac arrhythmias, cardiac enlargement, circulatory collapse, congestive heart failure, fat embolism, hypertension, hypertrophic cardiomyopathy in premature infants, myocardial rupture following recent myocardial infarction (see WARNINGS), pulmonary edema, syncope, tachycardia, thromboembolism, thrombophlebitis, vasculitis.
Dermatologic: Acne, allergic dermatitis, cutaneous and subcutaneous atrophy, dry scaly skin, ecchymoses and petechiae, edema, erythema, hyperpigmentation, hypopigmentation, impaired wound healing, increased sweating, lupus erythematosus-like lesions, purpura, rash, sterile abscess, striae, suppressed reactions to skin tests, thin fragile skin, thinning scalp hair, urticaria.
Endocrine: Decreased carbohydrate and glucose tolerance, development of cushingoid state, glycosuria, hirsutism, hypertrichosis, increased requirements for insulin or oral hypoglycemic agents in diabetes, manifestations of latent diabetes mellitus, menstrual irregularities, secondary adrenocortical and pituitary unresponsiveness (particularly in times of stress, as in trauma, surgery, or illness), suppression of growth in pediatric patients.
Fluid and electrolyte disturbances: Congestive heart failure in susceptible patients, fluid retention, hypokalemic alkalosis, potassium loss, sodium retention.
Gastrointestinal: Abdominal distention, bowel/bladder dysfunction (after intrathecal administration [see WARNINGS: Neurologic]), elevation in serum liver enzyme levels (usually reversible upon discontinuation), hepatomegaly, increased appetite, nausea, pancreatitis, peptic ulcer with possible perforation and hemorrhage, perforation of the small and large intestine (particularly in patients with inflammatory bowel disease), ulcerative esophagitis.
Metabolic: Negative nitrogen balance due to protein catabolism.
Musculoskeletal: Aseptic necrosis of femoral and humeral heads, calcinosis (following intra-articular or intralesional use), Charcot-like arthropathy, loss of muscle mass, muscle weakness, osteoporosis, pathologic fracture of long bones, post injection flare (following intra-articular use), steroid myopathy, tendon rupture, vertebral compression fractures.
Neurologic/Psychiatric: Convulsions, depression, emotional instability, euphoria, headache, increased intracranial pressure with papilledema (pseudotumor cerebri) usually following discontinuation of treatment, insomnia, mood swings, neuritis, neuropathy, paresthesia, personality changes, psychiatric disorders, vertigo. Arachnoiditis, meningitis, paraparesis/paraplegia, and sensory disturbances have occurred after intrathecal administration. Spinal cord infarction, paraplegia, quadriplegia, cortical blindness, and stroke (including brainstem) have been reported after epidural administration of corticosteroids (see WARNINGS:Serious Neurologic Adverse Reactions with Epidural Administration and WARNINGS:Neurologic).
Ophthalmic: Exophthalmos, glaucoma, increased intraocular pressure, posterior subcapsular cataracts, rare instances of blindness associated with periocular injections.
Other: Abnormal fat deposits, decreased resistance to infection, hiccups, increased or decreased motility and number of spermatozoa, malaise, moon face, weight gain.
بیش از حد مصرف
Treatment of acute overdosage is by supportive and symptomatic therapy. For chronic overdosage in the face of severe disease requiring continuous steroid therapy, the dosage of the corticosteroid may be reduced only temporarily, or alternate day treatment may be introduced.
Arze-Ject-A Dosage and Administration
عمومی
NOTE: CONTAINS BENZYL ALCOHOL (see PRECAUTIONS).
The initial dose of Kenalog-40 Injection may vary from 2.5 mg to 100 mg per day depending on the specific disease entity being treated (see DOSAGE section below). However, in certain overwhelming, acute, life-threatening situations, administration in dosages exceeding the usual dosages may be justified and may be in multiples of the oral dosages.
IT SHOULD BE EMPHASIZED THAT DOSAGE REQUIREMENTS ARE VARIABLE AND MUST BE INDIVIDUALIZED ON THE BASIS OF THE DISEASE UNDER TREATMENT AND THE RESPONSE OF THE PATIENT. After a favorable response is noted, the proper maintenance dosage should be determined by decreasing the initial drug dosage in small decrements at appropriate time intervals until the lowest dosage which will maintain an adequate clinical response is reached. Situations which may make dosage adjustments necessary are changes in clinical status secondary to remissions or exacerbations in the disease process, the patient’s individual drug responsiveness, and the effect of patient exposure to stressful situations not directly related to the disease entity under treatment. In this latter situation it may be necessary to increase the dosage of the corticosteroid for a period of time consistent with the patient’s condition. If after long-term therapy the drug is to be stopped, it is recommended that it be withdrawn gradually rather than abruptly.
مقدار مصرف
SYSTEMIC
The suggested initial dose is 60 mg, injected deeply into the gluteal muscle. Atrophy of subcutaneous fat may occur if the injection is not properly given. Dosage is usually adjusted within the range of 40 mg to 80 mg, depending upon patient response and duration of relief. However, some patients may be well controlled on doses as low as 20 mg or less.
Hay fever or pollen asthma: Patients with hay fever or pollen asthma who are not responding to pollen administration and other conventional therapy may obtain a remission of symptoms lasting throughout the pollen season after a single injection of 40 mg to 100 mg.
In the treatment of acute exacerbations of multiple sclerosis, daily doses of 160 mg of triamcinolone for a week followed by 64 mg every other day for one month are recommended (see PRECAUTIONS: Neuro-Psychiatric).
In pediatric patients, the initial dose of triamcinolone may vary depending on the specific disease entity being treated. The range of initial doses is 0.11 to 1.6 mg/kg/day in 3 or 4 divided doses (3.2 to 48 mg/m2bsa/day).
For the purpose of comparison, the following is the equivalent milligram dosage of the various glucocorticoids:
| Cortisone, 25 | Triamcinolone, 4 |
| Hydrocortisone, 20 | Paramethasone, 2 |
| Prednisolone, 5 | Betamethasone, 0.75 |
| Prednisone, 5 | Dexamethasone, 0.75 |
| Methylprednisolone, 4 | |
These dose relationships apply only to oral or intravenous administration of these compounds. When these substances or their derivatives are injected intramuscularly or into joint spaces, their relative properties may be greatly altered.
LOCAL
Intra-articular administration: A single local injection of triamcinolone acetonide is frequently sufficient, but several injections may be needed for adequate relief of symptoms.
Initial dose: 2.5 mg to 5 mg for smaller joints and from 5 mg to 15 mg for larger joints, depending on the specific disease entity being treated. For adults, doses up to 10 mg for smaller areas and up to 40 mg for larger areas have usually been sufficient. Single injections into several joints, up to a total of 80 mg, have been given.
مدیریت
GENERAL
STRICT ASEPTIC TECHNIQUE IS MANDATORY. The vial should be shaken before use to ensure a uniform suspension. Prior to withdrawal, the suspension should be inspected for clumping or granular appearance (agglomeration). An agglomerated product results from exposure to freezing temperatures and should not be used. After withdrawal, Kenalog-40 Injection should be injected without delay to prevent settling in the syringe. Careful technique should be employed to avoid the possibility of entering a blood vessel or introducing infection.
SYSTEMIC
For systemic therapy, injection should be made deeply into the gluteal muscle (see WARNINGS). For adults, a minimum needle length of 1½ inches is recommended. In obese patients, a longer needle may be required. Use alternative sites for subsequent injections.
LOCAL
For treatment of joints, the usual intra-articular injection technique should be followed. If an excessive amount of synovial fluid is present in the joint, some, but not all, should be aspirated to aid in the relief of pain and to prevent undue dilution of the steroid.
With intra-articular administration, prior use of a local anesthetic may often be desirable. Care should be taken with this kind of injection, particularly in the deltoid region, to avoid injecting the suspension into the tissues surrounding the site, since this may lead to tissue atrophy.
In treating acute nonspecific tenosynovitis, care should be taken to ensure that the injection of the corticosteroid is made into the tendon sheath rather than the tendon substance. Epicondylitis may be treated by infiltrating the preparation into the area of greatest tenderness.
How is Arze-Ject-A Supplied
Kenalog®-40 Injection (triamcinolone acetonide injectable suspension, USP) is supplied in vials providing 40 mg triamcinolone acetonide per mL.
| 40 mg/mL, 1 mL vial | NDC 0003-0293-05 |
| 40 mg/mL, 5 mL vial | NDC 0003-0293-20 |
| 40 mg/mL, 10 mL vial | NDC 0003-0293-28 |
ذخیره سازی
Store at controlled room temperature, 20°–25°C (68°–77°F), avoid freezing and protect from light. Do not refrigerate.
Bristol-Myers Squibb Company
Princeton, NJ 08543 USA
Product of Spain
1221153A5
Revised: August 2011
NDC 0003-0293-05 Rx only
KENALOG®-40
(Triamcinolone Acetonide
Injectable Suspension, USP)
40 mg per mL
1 mL Single Dose Vial
NDC 61219-821-01 Rx-Only
Arze-Ject-A
Kit Contains:
3 Kenalog-40 ® (1mL)
6 Isopropyl Alcohol 70% Prep Pads
1 Pair Nitrile Powder Free Sterile Gloves (Size: Large)
1 Adhesive Bandage
Sterile 4×4 Gauze
توزیع شده توسط:
Integrated Pharma Solutions LLC
Arlington, VA 22215
بسته بندی


| Arze-Ject-A kenalog kit |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
| Labeler – Integrated Pharma Solutions LLC (049528220) |
سوالات متداول
- آیا می توان از تریامسینولون استونید B برای درمان بثورات شدید پوشک روی یک دختر کوچک استفاده کرد؟














نظرات کاربران